Tekintse meg az e médiumban megjelent cikkeket és tartalmakat, valamint a tudományos folyóiratok e-összefoglalóit a megjelenés idején
Figyelmeztetéseknek és híreknek köszönhetően mindig tájékozott maradjon
Hozzáférhet exkluzív promóciókhoz az előfizetéseken, az indításokon és az akkreditált tanfolyamokon
A Neurology a spanyol Neurológiai Társaság hivatalos folyóirata, és 1986 óta tudományos közleményeket közöl a klinikai és kísérleti neurológia területén. A neurológiai tartalom a neuroepidemiológiától, a neurológiai klinikától, a neurológiai menedzsmenttől, a segítségnyújtástól és a terápiától kezdve a neurológiai alapkutatásig terjed. A folyóiratok tárgyi területei a gyermekneurológia, a neuropszichológia, a neurorehabilitáció és a neurogeriatrika. A Neurology-ban megjelent cikkek kettős-vak áttekintési folyamatot követnek, így a műveket minőségük, eredetiségük és érdeklődésük szerint választják ki, és így javítási folyamatnak vetik alá őket. A cikk formátuma tartalmazza a szerkesztőségeket, az eredeti dokumentumokat, az ismertetőket és a szerkesztőhöz intézett leveleket, a neurológia elismert minőségű tudományos információs eszköz az ideggyógyászat iránt érdeklődő, spanyolul használó szakemberek számára, amint azt a világ legrangosabb és legszelektívebb bibliográfiai indexei is tartalmazzák.
Indexelve:
MEDLINE, EMBASE, Web of Science, kibővített tudományos hivatkozási index, riasztási szolgáltatások és idegtudomány, idegtudományi hivatkozási index, ScienceDirect, SCOPUS, IBECS és MEDES
Kövess minket:
Az impakt faktor az előző két évben a kiadványban megjelent művek átlagosan egy évben kapott idézetek számát méri.
A CiteScore a közzétett cikkenként kapott idézetek átlagos számát méri. Olvass tovább
Az SJR egy tekintélyes mutató, amely azon az elképzelésen alapul, hogy az összes idézet nem egyenlő. Az SJR a Google oldalrangjához hasonló algoritmust használ; a publikáció hatásának mennyiségi és minőségi mértéke.
A SNIP lehetővé teszi a különböző tantárgyakból származó folyóiratok hatásának összehasonlítását, korrigálva az idézés valószínűségében a különböző tantárgyak folyóiratai között fennálló különbségeket.
- Összegzés
- Kulcsszavak
- Absztrakt
- Kulcsszavak
- Összegzés
- Kulcsszavak
- Absztrakt
- Kulcsszavak
- Bibliográfia
A májfibrózis és annak utolsó szakasza, a cirrhosis, óriási globális egészségügyi problémát jelent. A hepatikus encephalopathia (HE) vagy a portoszisztémás encephalopathia a cirrhosis hosszú távú klinikai állapota. Ez az áttekintés kiemeli a HD molekuláris alapjait, valamint az oxidatív stressz szerepét e betegség kialakulásában.
Számos tanulmány azt mutatja, hogy a HE multifaktoriális eredetű, a vér-agy gátjának változásai, az olyan anyagok, mint az ammónium és a mangán, valamint a dopamin, a glutamát és a GABA neurotranszmissziójának változásai szerepet játszanak e betegség patogenezisében.
A HD az akut és a krónikus májelégtelenség súlyos szövődménye. Neuropatológiailag asztrocita-változások, az Alzheimer-kór II. Típusú asztrocitózisaként ismertek, és specifikus asztrocita-fehérjék, például glia fibrilláris savas fehérje, glutamin-szintetáz, monoamin-oxidáz-gátlók és perifériás benzodiazepin receptorok megváltozott expressziója jellemzi.
A HD egy komplex neuropszichiátriai szindróma, amely májelégtelenséggel jár. Ezek a változások az oxidatív stressz megnövekedésének eredménye az agyban, a neurotoxinok hatása következtében. A HE kezelésének fő stratégiája az ammónia csökkentésére irányul, akár annak felszívódásának/termelésének csökkentésével, akár eliminációjának elősegítésével.
A májfibrózis és annak végstádiuma, a cirrhosis világszerte óriási egészségügyi probléma. A hepatikus encephalopathia (HE) vagy a portál-szisztémás encephalopathia továbbra is a hosszú távú cirrhosis egyik fő klinikai problémája. Ebben az áttekintésben hangsúlyozzuk a HE molekuláris alapját és az oxidatív stressz szerepét a betegség kialakulásában.
Számos tanulmány azt sugallja, hogy a HE patogenezise multifaktoriális lehet, és különböző tényezőket vonhat maga után, mint például a vér-agy gátjának, anyagainak megváltozása; például ammónia és mangán, neurotranszmissziós rendellenességek, például dopamin, glutamát és GABA.
A HE az akut és a krónikus májelégtelenség súlyos szövődménye. Neuropatológiailag asztrocita-változások jellemzik, amelyek Alzheimer-típusú II. Típusú asztrocitózis néven ismertek. Ezenkívül az asztrociták megváltoztatják az asztrocita-specifikus fehérjék, például glia fibrilláris savas fehérje, glutamin szintetáz, monoamin-oxidáz és perifériás típusú benzodiazepin receptorok megváltozott expresszióját.
A HE egy komplex neuropszichiátriai szindróma, amely májelégtelenséggel jár. Ezek a változások az agyban a neurotoxin aktivitás következtében fellépő oxidatív stressz növekedésének termékei. A HE kezelésének fő stratégiája az ammónia csökkentésére irányul, amely vagy abszorpciójának/termelésének csökkentésével, vagy eltávolításának növelésével érhető el.
A máj encephalopathia klinikai fokozatai.
| I. fokozat | A tudatosság hiánya, eufória vagy szorongás és csökkent figyelem |
| Évfolyam II | Letargia, apátia, az idő és a tér minimális dezorientálása, a személyiség változásai és a nem megfelelő viselkedés |
| Évfolyam III | Álmosság, zavartság és dezorientáció |
| Évfolyam IV | Eszik |
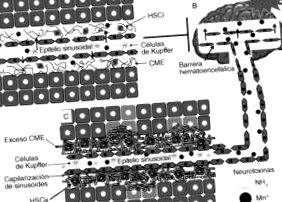
A HD patogenezise magában foglalja a neurotoxinok, például az ammónium és a mangán hatását, különféle jelenségek mellett, amelyek magukban foglalják a neurotranszmisszió változását, a vér-agy gát permeabilitását vagy az energia-anyagcserét (2. ábra). Noha a HE patogenezise bonyolult és még nem teljesen ismert, számos állatmodellt alkalmaztak e betegség kialakulásának tanulmányozására. Ezenkívül a sejt- és molekuláris biológia modern technikáinak megjelenése, valamint a képalkotó technikák neurofiziológiában történő alkalmazása jelentős előrelépéseket tett lehetővé a HE 16 patogenezisének megértésében. .
A máj encephalopathia kialakulásának változásai. A normális agyműködés több szempontból is függ a máj normális működésétől. Noha az agyat a vér-agy gát védi a neurotoxikus anyagoktól (az agyi erek jellemzője, amely megakadályozza sok vegyület átjutását a vérből az agyszövetbe), egyes neurotoxinok átjuthatnak ezen a gáton a máj sérülése után. mint a cirrhosis. Ez a májbetegség megnöveli a neurotoxikus anyagok, például az ammónium és a mangán mennyiségét, amelyek viszont oxidatív stresszt váltanak ki a vér-agy gáton való áthaladással, a neurotranszmisszió károsodásával, az energiaszintézis kudarcával és végül a sejthalállal.
Az asztrociták az agykéreg térfogatának körülbelül egyharmadát foglalják el, és szegregációs gátat képeznek a külső környezetben található idegsejtek számára. Részt vesznek az agy működéséhez elengedhetetlen különféle folyamatokban, fenntartják és szabályozzák az extracelluláris környezetet, részt vesznek a szabad gyökök felvételében, a fémek visszatartásában, az immunválasz és a gyulladás modulálásában, és befolyásolják az idegsejtek ingerelhetőségét és a neurotranszmissziót. Ezek a sejtek különböző morfológiai változásokat mutatnak: Májcirrhosis során Alzheimer-típusú II típusú asztrocitózis lép fel, akut májelégtelenség esetén pedig az asztrociták duzzadt sejteket mutatnak. A HD-ben lévő asztrociták dokumentáltan megváltoztatták az asztrocita-specifikus fehérjék expresszióját, mint például a glia fibrilláris savas fehérje (GFAP), az enzimek, például a glutamin-szintetáz (GS), a monoamin-oxidáz (MAO) inhibitorok és a perifériás benzodiazepin receptorok (PBR) 19 .
Az asztrociták szerepe
A központi idegrendszer (CNS) különböző sejttípusai közül az asztrociták az extracelluláris fehérjék és az adhéziós molekulák fontos forrása. Ezek központi szerepet játszanak a glia hegképződésében számos sérülés után, hogy megőrizzék a szövetek integritását és körülhatárolják a sérülés területét az reaktív asztrogliózisnak nevezett folyamatban. Az elváltozás körüli gliás heg megpróbálja megmenteni az egészséges központi idegrendszeri szöveteket a másodlagos elváltozásoktól; ugyanakkor gátolja a sérülés utáni esetleges axonális regenerációt 20 .
Az idegsejtek szerepe
Az asztrocitákban leírt morfológiai változásokkal ellentétben az idegsejtek nem mutatnak változásokat sejtfelépítésükben HD alatt. Krónikus májkárosodásban szenvedő betegek agyának hisztopatológiai vizsgálata során normális körülmények között és mennyiségben figyelnek meg idegsejteket, és a neuronok integritásának egyes markerei, például az N-acetil-szpartát nem változnak ezeknél a betegeknél. A HD állatmodelljeivel végzett vizsgálatok meggyőző bizonyítékot szolgáltatnak arra vonatkozóan, hogy az idegsejtek halálának mechanizmusai hasonlóak az iszkémiában megfigyeltekhez. Ezek a mechanizmusok magukban foglalják az NMDA receptor által közvetített excitotoxicitást, az oxidatív/nitrozatív stresszt, a tejsavas acidózist és a gyulladásgátló citokinek jelenlétét. .
Ammónium. Az ammónium (NH3) a legfontosabb neurotoxin, amely részt vesz a HD patogenezisében. Az elmúlt években fontos előrelépés történt annak meghatározása érdekében, hogy milyen szerepet játszik az agyi ödéma kialakulásában a fulmináns májelégtelenség alatt 13,22,23. Az ammónium infúziók alkalmazása patkányokban azt mutatta, hogy az agyi ödéma és a koponyaűri magas vérnyomás kísérletileg kiváltható, és ez a jelenség gátolható a GS-gátló metoximin-szulfát beadásával. Ez arra a koncepcióra vezetett, hogy a központi idegrendszerből származó glutamin részt vesz az ammónium méregtelenítésében azáltal, hogy ozmotikus gradienst eredményez a vér-agy gáton keresztül, ami agyödémához és asztrocita duzzanathoz vezet. Az agyban az ammóniának való kitettség következtében bekövetkező strukturális és neurokémiai változások intenzív kutatások tárgyát képezték. Az ammónium asztrogliális változásokat indukál, amelyek hozzájárulnak a sejtek duzzadásához az intracelluláris glutamin növelésével, amely olyan változásokat eredményez a vér-agy gátban, amelyek befolyásolják a glutamaterg neurotranszmissziót és növelik az idegsejt nitrogén-oxid szintetáz expresszióját 22 .
A dopaminerg neurotranszmisszió diszfunkciója
A hamis neurotranszmitterek felhalmozódásának okát a HD-ben a DA csökkenésének mechanizmusának tekintik. A megnövekedett DA konverzió encephalopathiás betegeknél növeli az aromás aminosavak, a fenilalanin és a tirozin koncentrációját az agyban, a DA neurotranszmitter mindkét prekurzorát. Ezenkívül leírták, hogy az Mn 2+ megváltoztatja a dopaminerg transzmissziót a DA konverzió növekedésével. .
A glutamát aminosav és az egyik aminosav neurotranszmitter az agyban, gerjesztő hatással. Alapvetően egy központi szénatomból áll, amely egy karboxilcsoporthoz (COOH) és egy aminocsoporthoz (NH3) kapcsolódik. Az agy-glutamát kizárólag endogén forrásokból származik; főleg ketoglutarátból, a Krebs-ciklus 37 termékéből. A neuronális glutamát neurotranszmitterként működik az idegsejtek közötti kommunikáció során. Ezek az idegsejtek lehetnek gerjesztő vagy gátló hatásúak. Az emlősök agyában és gerincvelőjében a glutamát gerjesztő hatása az 1950-es évek óta ismert, 37 de a gerinceseknél csak az 1970-es évek végén ismerték el a glutamátot az idegrendszer fő gerjesztő adóként 38 .
A gamma-aminosavsav (GABA) a domináns gátló neurotranszmitter az emlős központi idegrendszerében. A GABAerg neurotranszmisszió megváltozása számos neurológiai és neuropszichiátriai betegség, például epilepszia, skizofrénia, neurodegeneratív betegségek, alvászavarok és máj encephalopathia patofiziológiájában vesz részt. A GABAerg neurotranszmissziót a GABA közvetíti, amely aktiválja a posztszinaptikus GABA A receptor komplexet (GRC), a klorid-szelektív ioncsatornák specifikus ligandumát, aktiválás után a csatorna kinyílik, és lehetővé teszi a klorid bejutását a posztszinaptikus neuron gátlásához. A HD-ben a GABAerg neurotranszmisszió módosítását több mint két évtizeddel ezelőtt javasolták 39 .
A máj encephalopathia kezelése
A máj encephalopathia kezelésére használt gyógyszerek.
- A kutya krónikus bronchitisének fő szempontjai - Ateuves, az állatorvosi asszisztens számára
- 10 tipp a ci enyhítésére; etika
- A ló etetése fontos szempontok - TUXE Life
- Sebészet; a és az Est Medicine; tica Barcelonában, Granollers és Reus Cl; egyszeres C; nons Testterápia
- C; hogyan lehet megérteni az anális eredményeit; női hormonetika