1 Kutatóintézeti Kórház 12 de Octubre (i + 12) - Orvostudományi Kar - Madridi Complutense Egyetem (Spanyolország)
Másrészt a differenciált pajzsmirigyrák előfordulása, a relapszus megelőző terápiával végzett pajzsmirigyhormon-szuppresszió kísérleti in vivo modellje jelentősen megnőtt. Klinikai iránymutatások vannak a kezelésére, de nyilvánvaló, hogy a lehetséges származtatott másodlagos hatások pontos indikációt igényelnek, amely igazodik a pajzsmirigyhormonok hosszú távon előírt adagolásának kockázat-haszon arányához, különösen alacsony tumor agresszivitás esetén, magas korban, sőt törékeny betegeknél is. A nagy kockázatú betegeket csontdenzitometriára kell irányítani, hogy mérlegeljék a jövőbeni törések kezelését. Az osteoporosis megelőzése, különösen posztmenopauzában lévő nőknél, nagyon kívánatos, és szükség esetén megfelelő étrendet kell tartalmaznia a kalcium- és D-vitamin-kiegészítőkben. Még nincs egyetértés a pajzsmirigyrákban szenvedő betegek csontritkulásának kezeléséről és a szuppresszív kezelésről, de a postmenopausás osteoporosisra jelölt kritériumok általában alkalmazhatónak tűnnek.
KulcsszavakВ differenciált pajzsmirigyrák; kettős foton-denzitometria; csontsűrűség; trabecularis csont pontszám; hyperthyreosis és szubklinikai hypothyreosis; tirotrop hormon
Az elmúlt években előrelépés történt a csontváz fejlődésének és a felnőttek csonttömegének fenntartásának szabályozásában a hipotalamusz-hipofízis-pajzsmirigy tengely által. Tanulmányokat végeztek a pajzsmirigyhormonok osteoblastokra, osteoclastokra és chondrocytákra gyakorolt hatásáról. Ez a kutatás jobb genetikai ismereteket eredményezett e hormonok sejtes hatásának fiziológiájában. Nemrégiben javasolták az osteoporosis lehetséges D2-dezodináz-beavatkozásait. A csontásványi méltóság, a csontminőség és a pajzsmirigyhormonokkal történő törések kockázata közötti kapcsolat a normális posztmenopauzás nőknél arra utal, hogy ezek a hormonok szerepet játszanak még a normál pajzsmirigy tartományában is, ezekben a betegségekben.
Másrészt jelentősen megnőtt a differenciált pajzsmirigyrák, a terápiás kísérleti in vivo pajzsmirigyhormon-szuppresszió, a visszatérő betegség előfordulása. Vannak kezelési útmutatók, de egyértelmű, hogy a másodlagos származékok pontos egyensúly-korrigált indikációt, a pajzsmirigyhormon-dózis kockázat-haszon arányát igénylik, hosszú távra előírva, különösen alacsony tumor agresszivitás, előrehaladott életkor és még törékeny betegek esetén is. A nagy kockázatú betegeket csontdenzitometriára kell irányítani, hogy fontolóra vegyék a jövőbeni törések kezelését. Az osteoporosis megelőzése, különösen posztmenopauzás nőknél, nagyon kívánatos, és ennek megfelelő étrendet kell tartalmaznia a kalcium és a D-vitamin pótlásában, ha szükséges. Még mindig nincs egyetértés a pajzsmirigyrákban szenvedő betegek osteoporosisának kezelésében és a szuppresszív kezelésben, de úgy tűnik, hogy a posztmenopauzális osteoporosis feltüntetett kritériumai általában alkalmazhatók.
KulcsszavakВ pajzsmirigy rák; kettős foton denzitometria; csontsűrűség; trabecularis csont pontszám; hyperthyreosis és szubklinikai hypothyreosis; tirotróf hormon
A pajzsmirigyhormonok (HT) beavatkoznak a csontváz fejlődésébe, a csonttömeg csúcsának megszerzésébe és a csont átalakításának fenntartásába. Klinikai-epidemiológiai vizsgálatok azt mutatják, hogy a HT hiánya és a túlsúly is összefügg a törések kockázatával, tekintve, hogy az euthyreoidizmus elengedhetetlen a csont átalakulásának normális működéséhez [1].
Ebben a munkában áttekintjük a HT csonton kifejtett sejtes hatásait, különös tekintettel a pajzsmirigy-stimuláló hormon (TSH) feleslegének és szuppressziójának in vivo kísérleti modelljére nőknél differenciált pajzsmirigyrákban (DTC) szenvedő betegeknél, pre- és postmenopauzában. CDT-ben szenvedő férfiaknál nincsenek minőségi longitudinális vizsgálatok elemzésükre.
Pajzsmirigyhormonok és csont
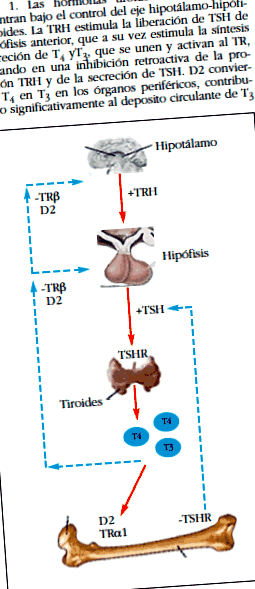
A HT-k és a csont szorosan kapcsolódnak egymáshoz, mivel a HT-k a csont átalakításának kulcsszabályozói. A HT alapvető szerepet játszik a gerincesek növekedésében és fejlődésében. A HT-k a pajzsmirigyben szintetizált jodotironinok, amelyek állandó szekrécióját két mechanizmus biztosítja: 1) a HT visszaható mechanizmus által vezérelt szekréciója a hipotalamusz-hipofízis-pajzsmirigy tengelyéből (1. és 2. ábra) intracelluláris aktivációval, amelyet Szövet-jodotironin-jód-dinázok [2].
A 2В T3 az oszteoblaszt közvetett hatására közvetetten hat az oszteoblaszt által közvetített hatással, amely valószínűleg a RANKL és a 6 és 8 interleukinek, valamint a PGE2 felszabadulását indukálja a korai szakaszban a prekurzorokon, vagy elősegíti a preoszteoklaszt differenciálódását. A T3 előnyben részesítené az oszteoblaszt differenciálódását és a mátrix mineralizációjának fázisait. Lehetséges, hogy az IGF-1 és transzporter fehérjéinek transzkripciója és más tényezők indukálása stimulálja az oszteoblaszt szaporodását és differenciálódását. A kondrocytán a TRО ± 1 és a TRОІ1 rendelkezésre állása ebben a sejtvonalban lehetővé teszi a T3 számára, hogy stimulálja érését és ezért az endokondrális csontosodás folyamatát. (Módosítva: Wojcika et al. 4) В
A HT receptorai
A HT-k ezen három funkcionális receptorát (TRО ± 1, TRОІ1 és TRОІ2) a THRО ± és a THRОІ gének kódolják, amelyek szabályozzák expressziójukat és transzkripciós válaszukat a TR-ekre. A csontban a TRО ± 1 és a TRОІ1 expresszióját írták le, az előbbi 10: 1 túlsúlyban volt. Ezért a TRО ± tekinthető a T3 csontra gyakorolt hatásának alapvető közvetítőjének [6].
HT, TSH és a csontok fejlődése
Mind a TRО ± 1, mind a TRОІ1 receptorok kifejeződnek a növekedési lemez kondrocitáin, ami arra utal, hogy ezek a T3-akció célpontjai. A kondrocita proliferációt és differenciálódást indiai sündisznó, PTHrp, BMP-R1A, IGF1, Wnt és FGF kontrollálja. Az első három negatív visszacsatolással indukálja a plakk növekedését és gátolja annak differenciálódását lineáris növekedésének szabályozásával. A HT-k beavatkoznak ebbe a szabályozásba, érzékenyek a T3 elérhetőségére, amely serkenti a gének expresszióját a porcmátrix szintéziséhez és az azt követő mineralizációhoz.
A THRО ± gén heterozigóta mutációját írták le a közelmúltban egy 6 éves kislánynál, akinek annak ellenére, hogy HT alacsony vagy normális határértéket és normális TSH-t mutat, növekedési retardációja és szövettani csont érintettsége hasonló volt a hypothyreosishoz, ami fontos ezen TRО ± receptorok szerepe az emberi csontfejlődésben [10].
HT és TSH a csont ásványi sűrűségével és töréseivel normál populációban
A hyperthyreosis kórtörténete kockázati tényezőnek tűnik. A SOF vizsgálatban (Osteoporotic Fractures Study of Osteoporotic Fractures) 192 idős nőnél 4,1 éves követéssel követték el a legmagasabb osteoporotikus törés előfordulási gyakoriságot azoknál a betegeknél, akiknek kórtörténetében voltak törések és/vagy pajzsmirigy-túlműködés [tizenöt]. Ebben a tanulmányban nem találtak bizonyítékot az alacsony TSH-szint és az alacsony BMD közötti kapcsolatra. A szerzők arra a következtetésre jutottak, hogy a hyperthyreosis csökkentheti vagy nem csökkentheti a csonttömeget, de tanulmányukban a BMD csökkenése nem volt felelős a korábbi hyperthyreosis és a csípőtörési kockázat közötti szoros összefüggésért.
HT és TSH: kapcsolat a csont ásványi sűrűségével és töréseivel pajzsmirigy-diszfunkcióban szenvedő nőknél
Összefoglalva, a közzétett adatok azt mutatják, hogy az egyértelmű ok-okozati összefüggés bizonyításához szignifikáns számú betegnél randomizált és kontrollált vizsgálatokra van szükség, valamint annak felmérésére, hogy a szubklinikai hyperthyreosisban a TSH szint normalizálása összefügg-e a törés kockázatával. Az adatok arra utalnak, hogy a szubklinikai hyperthyreosis a csípő és a nem csigolya törések megnövekedett kockázatával jár, de más tényezőket kell elemezni, és jobb minőségű vizsgálatokat kell végezni.
HT és csonttrabekuláris mikroarchitektúra
A differenciált pajzsmirigyrák TSH szuppressziójának kritériumai
A differenciált pajzsmirigyrák (DTC) a leggyakoribb endokrin neoplazia (az összes rák 1% -át teszi ki). A pajzsmirigyrák 85-90% -a CDT, amely két változatot foglal magában, a papilláris carcinoma (a leggyakoribb) és a follikuláris. Előfordulása az elmúlt 10 évben növekszik, de mortalitása változatlan maradt [29]. Ez a növekedés nagyrészt a diagnosztikai tesztek felbontásának növekedésének és javulásának tudható be, az esetleges mikrokarcinóma nagyobb mértékű kimutatásával.
A Tab1В TSH a hosszú távú pajzsmirigyhormon terápiára irányul differenciált pajzsmirigyrákban. Haugen BR és munkatársai szerint 32В
Note2tab1 ** A hiányos biokémiai válaszban szenvedő betegek TSH-értéke a kezdeti ATA-kockázattól, a Tg-szinttől, az időbeli Tg-trendtől és a szuppresszió kockázatától függően változhat.
Noha nincs általános egyetértés az optimális TSH-szintekről a relapszusok csökkentése érdekében, és a szubklinikus hyperthyreosis káros hatásainak minimalizálása mellett, az Amerikai Pajzsmirigy Szövetség (ATA) nemrégiben meghatározta a TSH-szuppresszió hatását CDT-ben szenvedő betegeknél, alacsony, közepes és magas a kiújulás kockázata a különféle klinikai tényezők figyelembevételével [32].
Tab2В: A TSH levotiroxinnal történő szuppressziójának a csont ásványi sűrűségére (BMD) gyakorolt longitudinális vizsgálati listája pajzsmirigyrákos pre- és postmenopauzás nőknélВ
A HT szuppresszív kezelése differenciált pajzsmirigy- és csontrák esetén. Hosszanti vs. keresztmetszetek
п »їA második áttekintett longitudinális vizsgálat Mulller és mtsai. [57] 15 menopauza előtti és 10 posztmenopauzás nőt vizsgáltak T4-szuppresszív kezeléssel, változó, 1,5 éves időtartam alatt. Ebből a csoportból 24 CDT-s beteg jutott, akiket DXA-val újraértékeltek 1,5 ± 0,5 éves követési intervallummal. 15 olyan kontrollalanyot választottak ki, amelyek nem, menopauzális állapot, életkor és BMI szerint egyeztek meg. Arra a következtetésre jutottak, hogy a TSH szuppresszióval az ágyéki BMD és a combnyak BMD nem szignifikáns csökkenése (2-5%) társult, incidens törések nélkül. A megállapított BMD csökkenés alacsonyabb, mint a Mazess által leírt klasszikus, amelyben a csigolyatörés megnövekedett kockázata 1,5-2-szeresére növekszik minden egyes szórásnál (SD), amelynél a BMD csökken [58], ami ezen a szinten nem mutat hatást.
Tapasztalataink szerint [55] 14 menopauza előtti és 13 posztmenopauzális nőt vizsgáltunk, akiket CDT és TSH szuppresszióval követtek a szolgálatunkban, a teljes pajzsmirigy-eltávolításuk óta két éven át ismételt kettős foton-denzitometriával. Betegeink 50% -ánál a TSH értéke 0,1 mIU/L alatt volt. Az LT4 dózis pozitív prediktív értéket mutatott minden vizsgált csonthelyen, amelyet alig írtak le. A vizsgált csont- és ásványianyag-paraméterek egyike sem korrelált a csonttömeggel, kivéve az alkalikus foszfatázt Ward háromszögének és ultradisztális sugarának szintjén. Ez összhangban van a normális BMD-vel és a csontok átalakulásának értékével, amelyet ezeknél a betegeknél tartósan elnyomó kezelések mellett találtak. Az elnyomott betegeknél a BMD kismértékű csökkenése mutatkozott a sugár disztális 1/3-ában (Z-pontszám = -0,77 ± 0,98; 95 CI: -1,11; -0,44), és nem volt különbség a menopauza előtti és utáni időszakban.
Papilláris CDT-vel rendelkező posztmenopauzás betegek szelektív és meglehetősen nagy csoportjában Sugitani és mtsai. [63] elemezte azt a hatást, amelyet a posztoperatív TSH szuppresszív terápia indukál a betegségektől mentes túlélésre, valamint annak hatását a BMD-re. Két csoportot elemeztek: 140 depressziós beteget (átlagos TSH: 0,07 ± 0,10 mIU/L, és 127 szuppresszió nélkül (átlag TSH: 3,14 ± 1,60 mIU/L). A nem elnyomott csoportból 120 beteg volt posztmenopauzás nők 5 évig követte, az ágyéki BMD csökkenését mutatta a posztmenopauzában lévő, 50 évnél idősebb nők alcsoportjában. Betegeik többsége alacsony kockázatú volt. Végül javasolják a TSH szuppresszióját, különösen alacsony kockázatú betegeknél és időseknél betegeket nem szabad feltüntetni, figyelembe véve azt is, hogy még a magas kockázatú betegeknél sem bizonyítottan csökkenti a kiújulást.
Karner et al. [64] egy évig CDT-ben szenvedő premenopauzás nőknél végezték. A TSH szuppresszió időtartama a vizsgálat kezdetén 9,4 ± 6,4 év volt, ezért hosszú. A BMD méréseket kétszer, egy év alatt végeztük el. A végtagok és a DXA SPA (single photon absorptiometry) alkalmazásával nem találták a BMD csökkenését a disztális sugár szintjén, sem az ágyéki és/vagy a csípő BMD-t. Rövid időtartamú longitudinális vizsgálat, kis számú (19 premenopauzás) alanydal. Fő ajánlása, hogy a TSH szuppresszív kezelés megkezdése előtt végezzen csontdenzitometriás vizsgálatot a csontritkulás magas kockázatának kitett betegek azonosítása érdekében.
Kockázati tényezők CDT és TSH szuppresszív kezelésben szenvedő betegeknél
- 25 év múlva az elhízás a nőknél több rákot okoz, mint a cigaretta
- Szakértők rámutatnak, hogy az elhízás összefügg a differenciált pajzsmirigyrákkal
- A méheltávolítás egy lehetőség az elhízott, méhrákos nők számára, a Diario Público
- Az emlőrákos menopauzás nőknél a hormonkezelés hatékonysága a testsúlytól függ
- Az elhízás megduplázza a vastagbélrák kockázatát a CuidatePlus nőknél