Tekintse meg az e médiumban megjelent cikkeket és tartalmakat, valamint a tudományos folyóiratok e-összefoglalóit a megjelenés idején
Figyelmeztetéseknek és híreknek köszönhetően mindig tájékozott maradjon
Hozzáférhet exkluzív promóciókhoz az előfizetéseken, az indításokon és az akkreditált tanfolyamokon
A Journal of Medicine and Research a Mexikói Állam Autonóm Egyetem tudományos kiadványa. Félévente spanyol és angol nyelvű cikkeket fogad el, és kiadványként fontolóra veszi az orvosi kutatással kapcsolatos összes művet. Eredeti cikkeket, áttekintő cikkeket, tudományos leveleket, klinikai irányelveket, konszenzust, szerkesztői megjegyzéseket, a szerkesztőkhöz intézett leveleket, az orvostudomány történetét és művészetét érintő cikkeket, tudományos jellegű cikkeket, amelyek a területek tartalmával rendelkező kutatási eredményeket tartalmaznak. kardiológia, pulmonológia, nephrológia, gasztroenterológia, reumatológia, nőgyógyászat, genetika, farmakológia, immunológia, molekuláris biológia, belgyógyászat, közegészségügy, általános orvoslás.
Journal of Medicine and Research az Universidad Autónoma del Estado de México tudományos folyóirata. Évente kétszer tesz közzé cikkeket spanyol és angol nyelven, és kiadás céljából figyelembe veszi azokat a műveket, amelyek az orvosi vizsgálattal kapcsolatosak. A folyóirat kiadványokhoz elfogad eredeti cikkeket, áttekintő cikkeket, tudományos leveleket, klinikai irányelveket, konszenzust, szerkesztői megjegyzéseket, szerkesztőkhöz intézett leveleket, cikkeket és az orvostudomány történelmét, ideértve a kardiológia, a pulmonológia területéről származó tudományos kutatási eredményeket, nephrológia, gasztroenterológia, reumatológia, nőgyógyászat, genetika, farmakológia, immunológia, molekuláris biológia, belgyógyászat, közegészségügy, általános orvoslás.
Kövess minket:
- Bevezetés
- Kórélettan
- Klinikai megnyilvánulások
- Diagnózis és kezelés
- Finanszírozás
- Bevezetés
- A leigh-szindróma fogalmi azonosítása
- A Leigh-szindróma biokémiai alapjai
- Kórélettan
- Klinikai megnyilvánulások
- Leigh-szindróma öröklődés
- Diagnózis és kezelés
- Finanszírozás
- Összeférhetetlenség
- Köszönöm
- Bibliográfia
A mitokondriumok felépítésének, fiziológiájának és rendellenességeinek vizsgálata számos tudós számára kutatási téma volt a történelem folyamán, utalhatunk arra az 1951-es évre, amelyben Denis Leigh leírja egy olyan esetet, amikor a gyermek saját klinikai megnyilvánulásai vannak a szindrómának. nevét viseli, amelyről egyre több ismeretes, de kevés előrelépés történt egy olyan kezelés kialakításában, amely képes megnövelni a szenvedők várható élettartamát.
Az emberi test, mint tökéletes gép, megköveteli a biológiai üzemanyagok (szénhidrátok, lipidek és fehérjék) hozzájárulását, amelyek szükségesek a különféle biológiai folyamatokhoz szükséges kémiai energia megszerzéséhez és ezáltal a homeosztázis fenntartásához. Ezeknek az üzemanyagoknak az anyagcseréjét a szervezetben különböző katabolikus és anabolikus utak alkalmazásával érik el, amelyekhez a sejtek összehangolt működése, vagyis a test bármely sejtjének organellái közötti jó kommunikáció szükséges.
A bioüzemanyagok helyes metabolizmusa után a sejtekben végül kémiai energiamolekulákat kapunk ATP formájában, amelyek szükségesek olyan folyamatok végrehajtásához, mint például; molekulák áthaladása a sejtmembránon, a flagellák mozgása, az izmok összehúzódása, sok más létfontosságú funkció mellett. Ennek a kémiai energiának a legnagyobb részét a mitokondriumok részvételével nyerik, amelyek felépítésében a fontos légzési lánc található az oxidatív foszforilezés és végül az ATP megszerzése érdekében.
A Leigh-szindróma fogalmi azonosítása
Neurodegeneratív rendellenesség, amelynek következménye a következők: Piruvát-dehidrogenáz-komplex, a légzőszervi lánc I., IV. Vagy V. komplexe 1 .
A Leigh-szindróma biokémiai alapjai
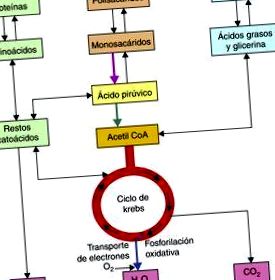
A szénhidrátok, a lipidek és a fehérjék katabolizmusában használt metabolikus utak az Acetyl CoA 2 molekulák végső képződése után a mitokondriumokban konvergálnak, amelyeket a trikarbonsav-ciklus metabolizál, majd redukált kofaktorok, NADH + H és FADH2 képződik. amelyek majd oxidálódnak a légzési láncban ATP-molekulák előállításához (1. ábra).
Acetil CoA megszerzése.
A szénhidrátok esetében mind az aerob, mind az anaerob glikolízis fontos útvonal ezeknek a molekuláknak az alkalmazásához, miután az anaerob glikolízis által a sejt citoszoljában rejlő reakciósorozat után elérjük a piruvátot, amely a piruvát-dehidrogenáz szubsztrátja lesz. komplex, amely oxidálja a piruvát molekulát Acetyl CoA-val a mitokondriumokban.
Az Acetyl CoA molekula az A koenzimből képződik, amelynek molekulája adenint, ribózt, pantoténsavat és tiolcsoportot tartalmaz, utóbbi reagál a karboxilcsoportokkal úgy, hogy végül az Acetyl CoA molekula létrejöjjön, ez egy nagy energiájú vegyület, így Ön adományozhatja acetilcsoportját a trikarbonsav ciklusban.
A trikarbonsav-ciklusban az acetil-CoA-molekula metabolizálódik CO 2-vá és H20-vá, hasonlóan ebben a ciklusban részt vevő reakciósorban; 3 NADH + H, 1 FADH 2 és egy GTP molekula. Az ebben a ciklusban termelődő redukált kofaktorok (NADH + H és FADH2) azért fontosak, mert a bioüzemanyagok katabolizmusa után nyert elektronok transzportereként működnek, ezért ezek a Krebsi ciklusból vagy trikarbonsavakból származó kofaktorok ezt követően adományozza ezeket az elektronokat a légzési lánc első komplexjéhez a NADH + H kofaktor esetében, vagy a Complex II-hez a FADH2 kofaktor esetében, miután egy sor reakciót ezek a kofaktorok oxidáltak és a komplexek redukálódtak ( 2. ábra).
A sejtcitoszol anaerob glikolízisében kapott redukált kofaktorok nem képesek átjutni a mitokondriális membránon, ezért belépésükhöz a glicerin - 3 - foszfát transzfert (főleg az agy és az izomsejtekben) és a malát - aszpartátot (főleg a májban és a szív), amelyek bevezetik a redukált kofaktorok elektronjait a citoplazmától a mitokondriumig.
Az elektronok áthaladása a légzési láncon az I vagy II komplexben kezdődik, később átjutnak az ubiquinon (Q), majd a III komplexbe, ez citokrómá redukálódik, végül a citokróm IV komplexgé redukálódik, amely 2 elektront adományoz az oxigénnek a Vízmolekula képződésénél meg kell jegyezni, hogy az elektronok áthaladása a légzési lánc enzimatikus komplexein keresztül abból a komplexből történik, amely alacsonyabb standard redukciós potenciált mutat, mint a magasabb standard redukciós potenciállal rendelkező komplex, azaz az alacsonyabb affinitással rendelkező elektronoktól a komplexek felé, amelyek iránti affinitásuk nagyobb.
Az elektronok áthaladása a légzési lánc komplexein keresztül párosul az I., III. És IV. Komplex protonjainak az intermembrán térbe történő pumpálásával, ezzel létrehozva egy elektrokémiai gradienst ebben a térben, a protonok hajlamát. stabilizálja a gradienst a belső mitokondriális membrán mindkét oldalán, ez lehetővé teszi számukra, hogy áthaladjanak az ATPáz komplexen, amelynek szerkezete egy F 1 és F 0 alegységen alapul. Az F 0 alegység képezi azt a csatornát, amelyen keresztül a protonok áthaladnak, míg az F 1 alegység az a hely, ahol ADP-ből és Pi-ből az ATP-molekula képződése zajlik, ezért fontos megjegyezni, hogy az az energia, amely ezen a csatornán áthaladó protonok lehetővé teszik a szubsztrátok (ADP és Pi) által képzett ATP-molekula felszabadulását, nem szabad azt gondolni, hogy a protonok átjutásával nyert energia megfelelő mértékben az ATP-ben található energia.
Az ATP-molekulák megszerzése után ezek felhasználhatók az élettani folyamatok széles körében, amelyek a megfelelő működéshez és az emberi létfontosságú egyensúly fenntartásához szükségesek.
A testben vannak olyan szövetek, amelyek kiemelkednek az intakt oxidatív anyagcsere követelménye miatt, amely biztosítja a funkció hatékony végrehajtásához szükséges energia megszerzését, ezeken a szöveteken belül a központi idegrendszer dominál, amelyeken belül kiemelkednek a bazális ganglionok magas metabolikus aktivitás bemutatásához olyan helyzet, amely kiszolgáltatottá teszi őket a sejtkárosodásokkal szemben, így ezeknek a struktúráknak a sejtanyagcseréjében bekövetkező kudarcok jelentősen tükröződnek a testben végzett ellenőrzési funkcióikban.
A bazális ganglionok (globus pallidus, putamen, caudate nucleus, subthalamus nucleus és substantia nigra) az idegsejtek felhalmozódásai, amelyek elsődleges feladata a mozgások kezdetének, amplitúdójának és gyorsaságának szabályozása, 4 egy Leigh-szindrómás gyermeknél, az oxidatív kudarc hiánya. ezen struktúrák anyagcseréje és nekrózisa mozgáshibákká alakul át, ezért motorhiány vagy a motoros rendszer rendellenes aktiválása jellemzi őket, ami merevséghez, remegéshez és akaratlan mozgásokhoz vezet (3. ábra).
Basalis ganglionokrózis.
Az ATP-termelés ebben a szindrómában bekövetkező csökkenése nem korlátozódik a központi idegrendszerre gyakorolt hatásaira, ennek az energiacsökkenésnek a következményei a Leigh-szindróma klinikai megnyilvánulásaiban tükröződnek.
Görcsrohamok, pszichomotoros retardáció, optikai atrófia, hipotónia, gyengeség, letargia, hányás, rendellenes mozgások (ataxia, remegés), ingerlékenység, látásvesztés és légzési rendellenességek 3 .
Leigh-szindróma öröklődés
Bár a mitokondriumnak megvan a maga DNS-je, nem független a nukleáris DNS részvételétől, mivel mindkettő részt vesz a légzési lánc egyes enzimatikus komplexeit alkotó alegységek kódolásában, a II. Komplex kivételével. kizárólag nukleáris DNS kódolja, ezért az érintett komplextől és annak kódolásától függően az öröklés típusa lehet: Anyai, mitokondriális DNS mutációk vagy Autosomális Recesszió esetén, amikor a mutációk a Nukleáris DNS-ben fordulnak elő 5 .
A leggyakrabban leírt Leigh-szindróma eseteit a mitokondriális DNS mutációival azonosították, amelynek génje az egyik ATPáz alegységet kódolja, ezért anyai öröklődést mutat, másrészt a nukleáris DNS mutációi, amelyek befolyásolják a Complex IV szindrómát autoszomális recesszív öröklődést mutat be. Ennek a szindrómának a megjelenési gyakorisága 36 000 születésből 1.
Diagnózis és kezelés
A szindróma klinikai megnyilvánulásai 6 hónapos kor előtt jelentkeznek, az esetet értékelő orvosnak nagy szakértelemre van szüksége ahhoz, hogy ezt a rendellenességet meg lehessen különböztetni más, hasonló jellemzőkkel rendelkező és összetéveszthető mitokondriális rendellenességektől a diagnózis érdekében. olyan erőforrásokat kell felhasználni, mint; Izombiopszia a légzési lánc működésének elemzéséhez és az enzimkomplexek hibájának azonosításához, valamint a mágneses rezonancia és a számítógépes tomográfia használata, amely lehetővé teszi a bazális ganglionok nekrózisának azonosítását, amely a Leigh-szindróma fő jellemzője.
A szindróma diagnosztizálása után a kezelés palliatív, ha ketogén étrendet alkalmaznak, amikor a szindróma piruvát-dehidrogenáz-hiányhoz kapcsolódik, akkor nem tükrözhet semmilyen hasznot, mivel nincs hatékony kezelés, amely lehetővé teszi a károk, a gyermek várható élettartamának csökkentését. ezzel a szindrómával nem haladja meg a 2 évet.
A cikk végrehajtásához szponzor nem érkezett.
Összeférhetetlenség
A szerző kijelenti, hogy nincs összeférhetetlenség.
Dr. Aurelio Mendoza Medellinnek, a Mexikói Állami Autonóm Egyetem Orvostudományi Karának biokémiai tanulási egységének professzorának a cikk elkészítéséhez hozzájáruló tudásért.
- S; Leigh-szindróma d-vel; komplexek hiánya I; A mitokondriális légzési lánc III. És IV
- HIRSCHSPRUNG BETEGSÉGÉNEK KEZELÉSE, GYÓGYLAP
- Journal of Holistic Medicine Complementary Medicines Nº 53
- Autonomy Personal Research Magazine
- Diéta kockázat; diszlipidémiák jelenléte az iskolás gyermekeknél Revista de Medicina e