Tekintse meg az e médiumban megjelent cikkeket és tartalmakat, valamint a tudományos folyóiratok e-összefoglalóit a megjelenés idején
Figyelmeztetéseknek és híreknek köszönhetően mindig tájékozott maradjon
Hozzáférhet exkluzív promóciókhoz az előfizetéseken, az indításokon és az akkreditált tanfolyamokon
A Skin egy folyóirat, amelynek célja a bőrgyógyászat továbbképzése. Emiatt érdeklődése nem korlátozódik a bőrgyógyászra, hanem kiterjed azokra az orvosokra, akik ebben a szakterületen indulnak, azokra, akik feladataikat nem a nagy kórházi központok látják el, valamint olyan nem szakorvosokra, akiknek naponta bőrgyógyászati problémákkal kell szembenézniük napi gyakorlatában. Ennek a célnak a teljesítése érdekében a folyóirat a következő részekkel tagolódik: Hírek, Vélemények, Iránymutató jelek/Differenciáldiagnosztika, A diagnózis esetei, A bőr a mindennapi gyakorlatban, A bőr az orvostudomány és szakterületeivel összefüggésben, Dermatológiai terápiák. A folyóirat szerkesztőségi bizottsága biztosítja a szigorúságot, a minõséget, a gyakorlati érdeklõdést és a didaktikai kapacitást a témák és a szerzõk gondos megválasztásának, valamint az alkalmazott táblázatok és ikonográfiák sokféleségének köszönhetõen.
Indexelve:
Kövess minket:
A CiteScore a közzétett cikkenként kapott idézetek átlagos számát méri. Olvass tovább
Az SJR egy tekintélyes mutató, amely azon az elképzelésen alapul, hogy az összes idézet nem egyenlő. Az SJR a Google oldalrangjához hasonló algoritmust használ; a publikáció hatásának mennyiségi és minőségi mértéke.
A SNIP lehetővé teszi a különböző tantárgyakból származó folyóiratok hatásának összehasonlítását, korrigálva az idézés valószínűségében a különböző tantárgyak folyóiratai között fennálló különbségeket.
1996-ban a nukleozid reverz transzkriptáz-gátló (NRTI), a proteáz-gátló (PI) és az ezt követően nem-nukleozid-gátló analógok alapján új kombinációs terápiákat vezettek be a HIV-1 fertőzés kezelésére. Reverz transzkriptáz (NNRTI). Ezen betegek hosszabb túlélésével egy új szindróma jelenik meg, amelyet a testzsír újraeloszlása és az anyagcsere-rendellenességek jellemeznek, az úgynevezett "HIV-betegek lipodisztrófiája" (LDHIV).
Az első leírt eset az 1997-es indinavir-kezeléssel volt összefüggésben 1; Később Carr és mtsai 2 részletesen meghatározták azt a szindrómát, amelyben a perifériás lipodystrophia megjelenik, a dyslipidaemia és az inzulinrezisztencia együtt a proteáz inhibitorokkal történő kezeléssel kapcsolatban.
Az LDHIV olyan folyamat, amelynek gyakorisága és súlyossága változó. A perifériás zsírvesztés túlnyomórészt néhány betegnél jelentkezik, míg mások metabolikus elváltozásokat mutatnak, mielőtt a morfológiai változások nyilvánvalóak lennének.
Mivel a zsírvesztés fokozatosan következik be hónapok vagy évek alatt, az LDHIV korai felismerése nehéz, különösen elhízott betegeknél és nőknél. A testzsír változásainak észlelésére számos kiegészítő módszert alkalmaztak, mint például számítógépes tomográfia, mágneses rezonancia képalkotás, ultrahangvizsgálat vagy kettős energiájú röntgenabszorpciós geometria (DEXA), bár egyik sem általánosan elfogadott.
Ha mindehhez hozzátesszük a megállapított diagnosztikai kritériumok hiányát vagy a konszenzusos kiegészítő tesztek hiányát, akkor nem meglepő, hogy az LDHIV prevalenciája ilyen változó (8 és 84% között, átlagosan 42%) 3. Az előfordulás az antiretrovirális kezelés időtartamával növekszik. Elhelyezkedését tekintve az arc a leggyakrabban érintett terület (45%), amelyet a végtagok (42%), a has (39%), a karok (39%), a fenék (36%) és a dorsocervicalis követ. régió (4%) 4 .
A testzsír újraelosztása
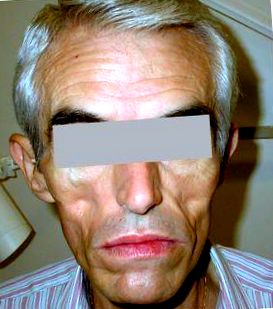
A zsírszövet szimmetrikusan csökken az arcból (1. ábra) és a végtagokból. Az érintett betegek hamis, izmos atlétikai megjelenést és jellegzetes macerás fácieseket mutatnak be. Egyes betegeknél ez a zsírvesztés egybeesik a zsírszövet felhalmozódásával a nyak körül, a dorsocervicalis gerincben ("bivalypúp") (2. ábra), a felső törzsben és az intraabdominális régióban 5. A zsigeri zsír növekedik, ezáltal fenntartva a testzsír-készletet a megfigyelt anyagcsere-változásokra reagálva.
1. ábra: Lipoatrophia az arcon.
2. ábra «Buffalo púp».
Néhány betegnél, különösen nőknél, mellnövekedést figyeltek meg, bár nem világos, hogy a zsír- vagy mirigyszövet rovására megy-e.
Ez a fenotípusos változás fontos fizikai megbélyegzést jelent ezeknek a betegeknek, és csökkentheti a terápiás adherenciát 6 .
A zsírszövet, amelyet klasszikusan energiatárolónak tekintenek, komplex endokrin, metabolikus és immunfunkciókat lát el. Az adipocita az egyetlen sejt, amely speciálisan alkalmas nagy mennyiségű zsírsav felhalmozására triacil-glicerin (TG) formájában. Más szövetek más mechanizmusokkal rendelkeznek a zsírsavfelesleg szabályozására. A máj képes átalakítani a TG-t nagyon kis sűrűségű lipoproteinekké (VLDL), és az izom az izomaktivitás növelésével csökkenti a lipidtartalmat. A hasnyálmirigy viszont csak kompenzatív béta-oxidációval rendelkezik, ezért a zsírsavfelesleg miatt kiszolgáltatottabb a lipoapoptosisnak, ami megmagyarázza a cukorbetegség megjelenését elhízott betegeknél 7 .
Adipociták hiányában, csakúgy, mint a lipodisztrófiáknál, a kis kalóriatúlsúlyok a TG lerakódását okozzák a nem zsírszövetekben, ennek következménye a máj steatosis, inzulinrezisztencia, nem inzulinfüggő diabetes mellitus és különböző fokú kardiomiopátia.
A proteázgátlókkal kezelt betegek 50-70% -ában dyslipidaemia alakul ki, míg a hiperglikémia a proteázgátlókkal kezelt betegek 20% -ában fordul elő, de 62% -uknál csökkent a glükóz tolerancia 8 .
Az NRTI-vel kezelt betegek 14% -ának hiperglikémiája és 7% -ának diabetes mellitusa van.
Az LDHIV-ben szenvedő betegeknél a „bölénypúp” inkább a hiperinsulinémiához, mint a diszlipidémiához kapcsolódik 9 .
Az antiretrovirális kezelés másodlagos metabolikus hatásai, mint például a dyslipidaemia és az inzulinrezisztencia, fokozzák az endothel károsodását és elősegítik a proatherosclerotikus állapotot 10,11. Ezért kerülnie kell az egyéb kockázati tényezőket, például a dohányzást, ellenőriznie kell a magas vérnyomást, és elő kell mozdítania a testmozgást és a megfelelő étrendet.
LDHIV KOCKÁZATTÉNYEZŐK
Proteáz inhibitorok
Az LDHIV megjelenését az összes proteázgátlóval, különösen az indinavirral, a ritonavirral és a szakvinavirral együtt írták le. Az LDHIV kumulatív valószínűségét 3,2% -ra becsülték a kezelés 6 hónapjában, 10,7% -ot a 12. hónapban, 62,5% -ot a 24. hónapban és 75% -ot a 30. hónapban. .
Nukleozid reverz transzkriptáz inhibitorok
Mind a lamivudin (3TC), mind a sztavudin (d4T) a testzsír rendellenes újraeloszlásához kapcsolódik, amely megkülönböztethető a proteáz-gátló betegeknél tapasztaltaktól. Ezek a betegek azonban súlycsökkenésről, kimerültségről, hányingerről, hepatomegalia, májműködési zavarokról és a tejsav-koncentrációkról is beszámolnak, amelyek jellemzőek a károsodott mitokondriális funkcióra 12 .
HIV-fertőzés
Az LDHIV kialakulása és súlyossága közvetlenül összefügg a HIV-fertőzés időtartamával. Az alacsony CD4-szám által meghatározott fertőzés súlyossága összefügg a lipoatrophia megjelenésével 13. A rendkívül aktív antiretrovirális kezelés (HAART) korai megkezdése a betegség kevésbé előrehaladott stádiumaiban minimalizálhatja az LDHIV kockázatát.
Táplálkozási állapot, életkor, nem és faj
Azoknál a betegeknél, akik túlsúlyosak, mielőtt a HAART-t proteázgátlókkal kapták volna, nagyobb valószínűséggel van egy bivalypúp és a mell megnagyobbodása, de kisebb az arc- és a gluteális lipoatrophia előfordulási gyakorisága, mint a nem túlsúlyos egyéneknél. Másrészt az alacsony testsúly a kezelés megkezdése előtt meghatározza a súlyosabb lipodystrophiát 14 .
Az idősebb betegek testtömeg-tömege általában nagyobb, ami módosíthatja az LDHIV-ben megfigyelt zsírelosztási változásokat. Ezzel szemben az életkor és az LDHIV közötti kapcsolatot a mitokondriális DNS-ben (mtDNS) az öregedéssel természetesen előforduló deléciók nagyobb száma közvetítheti 15 .
Az LDHIV-ben szenvedő nők derékabb androidos fenotípust szereznek: a csípő aránya jobban hasonlít a férfiakhoz, ami hiperinsulinémiával, hiperandrogenémiával, fokozott tesztoszteronszinttel és a lutropin: follitropin aránnyal és hiperlipidémiával jár együtt 16 .
A fehérek nagyobb kockázatot jelentenek az LDHIV-re nézve, mint az afroamerikaiak 17 .
LDHIV PATOGENEZIS
Az LDVIH-ra vonatkozóan számos kórokozó elméletet javasoltak, bár a legelterjedtebb a mitokondriális toxicitás. Az NRTI-k az adenozin, hisztidin, guanozin és timidin származékai, amelyek alternatív szubsztrátumokat biztosítanak a polimerázok számára. Az NRTI-k gátló hatása a polimerázokra nagyobb a HIV reverz transzkriptáz> pol-γ DNS> pol-β DNS> pol-α DNS = pol-ε DNS 18 esetében. Az mtDNS replikációját gamma-polimerázon keresztül hajtják végre, így az NRTI-k az mtDNS-t is befolyásolják.
A hibás mtDNS-replikáció a mitokondriális enzimek hibás aktivitását, az OXPHOS, a foszforilációs lánc megváltozását eredményezheti, ami növeli a laktáttermelést, amely mitokondriális apoptózisban végződik (3. ábra).
3. ábra: NRTI mitokondriális toxicitás, amely magában foglalja a légzési lánc megváltozását és a mitokondriális DNS kimerülését.
A mitokondriális gamma DNS-polimeráz befolyásolásának képessége nagyobb a zalcitabin> didanozin> sztavudin> lamivudin> tenofovir> zidovudin> abakavir 19 esetében. .
Kimutatták, hogy az NRTI-kezelés kvantitatív PCR-rel mérve összefügg az adipociták mtDNS-csökkenésével. A zidovudin átlagos kimerülése 52,1%, míg a sztavudiné 87,1% 20 .
CITOKINOK, ADIPOCINOK ÉS LDHIV
A különböző adipokinek plazmakoncentrációi vagy génexpressziója megváltozik az LDHIV-ben. A pro-gyulladásos citokinek plazma növekedése és az adipokinek zsírszövet általi expressziójának és/vagy termelésének megváltozása döntő fontosságú lehet ezeknél a betegeknél a zsír átalakításában és az anyagcserében. Az antiretrovirális kezelésben még nem részesült betegek zsírja megváltoztatja az adipokinek leptin és adiponectin gén expresszióját, valamint az adipocita differenciálódásban, az anyagcserében és a mitokondriális funkcióban részt vevőket. Ez megmagyarázná, hogy maga a HIV-1 első káros hatást gyakorol az adipocitára, és hogy később, antiretrovirális kezelés bevezetésével, a lipodistrofikus szindrómára jellemző morfológiai variációk fizikailag nyilvánvalóvá válnak 22 .
A keringő adiponektin mennyisége csökken a zsíreloszlásban szenvedő betegeknél, összehasonlítva a lipodystrophiával nem rendelkező betegek körében. Az alacsony adiponektin-koncentráció és az inzulinrezisztencia közötti összefüggés ismert, bár nem lehet meghatározni, hogy az említett metabolikus változás az adiponektin-csökkenés oka vagy következménye .
A leptin és az adiponektin mRNS helyi expressziója csökken az érintett betegek zsírjában, míg a tumor nekrózis faktor (TNF) alfa, interleukin (IL) 6 és IL-8 mRNS expressziója 25,26 .
A TNFα 238G/A promoter régiójának heterozigóta nagyobb valószínűséggel halad LDHIV-re, mint a nem heterozigóta betegek, 1,7-szer nagyobb kockázattal. .
A SREBP-1 (szterin-szabályozó elemkötő fehérje) 1c izoformájának stimulációs képessége az adipocita differenciálódásban ismert. Az SREBP-1c mRNS expressziója jelentősen csökken az LDHIV-ben szenvedő betegeknél, ami korrelál a csökkent adipogenezissel és az inzulinrezisztenciával 28 .
A proteázgátlók (kevesebb amprenavir) megváltoztatnák a lamin A/C érését, ami a mag architektúrájának megzavarását okozná, ami az SREBP-1c 29 mag diszlokációját és ezért adipocita diszfunkciót okozhat 30,31 .
A megnövekedett dorsocervicalis zsírban vagy a "bivaly púpban" a génexpresszió eltér az LDHIV-ben szenvedő betegek más helyein található zsíroktól, ami más patogenetikai mechanizmust jelez a zsír ezen lokalizált felhalmozódására 32 .
Megnövekedett szérum IFNα-koncentráció figyelhető meg lipodystrophiás betegeknél, pozitív korrelációban áll a koleszterin, trigliceridek, VLDL és az apolipoprotein B 33 szintjeivel. Az IFNα a zsírsejtekben közvetlen mechanizmus révén, vagy közvetett módon a hipotalamusz-hipofízis-mellékvese tengely stimulálásával, a kortizol, a noradrenalin és a glükagon koncentrációjának növelésével, valamint a triglicerid-clearance csökkentésével növeli a lipolízist. Összességében az IFNα hozzájárul az LDHIV-ben szenvedő betegeknél megfigyelt diszlipidémiához, és ezekben a betegeknél a lipidelváltozások legjobb markerként jelenik meg.
Habár az immunkonstitúciót az LDHIV patogén mechanizmusaként javasolták, a kezelt betegek testváltozásainak prospektív értékelése azt mutatja, hogy a végtag zsírvesztése a legnagyobb immun helyreállítása után következik be, így az etiológia nem valószínű az immun helyreállítására LDHIV-ben.
Összefoglalva, a különböző bizonyítékok szerint a proteázinhibitorok jobban összefüggenek a zsigeri zsír felhalmozódásával és a lipodystrophiás szindrómára jellemző metabolikus változásokkal, míg az NRTI-k mitokondriális toxicitást okoznak, és sokkal fontosabbak a perifériás zsírvesztés kialakulásában.
A proteáz inhibitorok szuszpenziója terápiás stratégiaként nem bizonyítottan hatékony a testzsír helyreállításában, bár az anyagcsere-változások javulhatnak. Az abakavirral végzett terápiás helyettesítés a zsírvesztés javulásával jár, bár ritkán látható 34 .
Néhány nagyobb lipodistrófia-termelő képességű antiretrovirális szer azonosítása azt jelenti, hogy a kezdetektől fogva különböző terápiás kezelési módokat fontolgatnak, és a jelenlegi tanulmányok új gyógyszerek kifejlesztésére irányulnak, amelyek kevésbé vagy egyáltalán nem befolyásolják az adipocytát.
A lipodystrophia létrejötte után számos kitöltési lehetőség áll rendelkezésre az LDVIH-ra jellemző szubkután térfogatvesztés helyreállítására.
Az L politejsavat 1999 óta hagyja jóvá Európában, az Egyesült Államokban pedig az Élelmiszer- és Gyógyszerügyi Hivatal (FDA) 2004 óta a HIV-vel összefüggő arc lipoatrophia kezelésében. A termék perzisztenciája legalább 3 év, és a 3 éves követés során észlelt egyetlen mellékhatás az esetek 11% -ában a szubkután papulák képződése volt, amely jobban tapintható, mint látható. .
Egy másik széles körben alkalmazott töltőanyag egy háromdimenziós térhálósított polimer, amely a polialkilimid családba tartozik (Bio Alcamid ®). Ez egy fizikailag stabil termék, amely beültetés után állandó biológiai kapszula kialakulását indukálja, ezért az endoprotézis fogalma. Lipofillinget is alkalmaznak, amely a beteg saját zsírátültetéséből áll, amelyet néha bonyolít egyes betegek súlyos lipoatrophiája 36 .
Központi elhízásban szenvedő betegek gyógykezeléseként a szomatotropint lipolitikus és oxidatív tulajdonságai miatt 4 mg/nap dózisban, 12 héten keresztül alkalmazták. A kezelést a hasi szubkután zsigeri zsír csökkenése, de a végtagok zsírjának csökkenése és a glükóz növekedése is kíséri. Ez utóbbi hatás fontos korlátozást jelent a szomatotropin alkalmazásában ezeknél a betegeknél, mivel rontaná az inzulinrezisztenciát 37 .
A tiazolidindionok, a PPARγ adipogén faktor agonistáinak alkalmazása előnyös lehet a lipoatrophia kezelésében és javíthatja az inzulinérzékenységet. Mindazonáltal a nagy sűrűségű lipoprotein-koleszterinszint csökkenése és az alacsony sűrűségű lipoprotein-koleszterinszint növekedése kíséri, ami súlyosbítja a lipodystrophiás szindrómára jellemző diszlipidémiát 38 .
Habár több patogenetikai mechanizmust javasoltak a HIV-1-hez társuló lipodisztrófiában, sok ismeretlen marad a testzsír ezen sajátos eloszlásának patogenezisében és az anyagcserezavarok megjelenésében. Valószínűleg több genetikai és virológiai tényező, maga a fertőzés és/vagy az immunkonstitúció által okozott masszív citokinek termelése, valamint a különböző antiretrovirális kezelések hatása együttesen avatkozik be ennek a lipodystrophiás szindrómának a kialakulásába.