Dr. Kepa Balparda egy 36 éves páciens esetét mutatja be, akit két évvel korábban, Panamában műtöttek az írisz színének megváltoztatása céljából. A beültetett eszköz az "Új színes írisz implantátum" volt. 15 évvel ezelőtt mindkét szemében a LASIK története volt.
A glaukóma és a szaruhártya dekompenzációjának kialakulása után az implantátumokat eltávolították, egy műtétet Kolumbiában hajtottak végre.
Abban az időben, amikor Dr. Balpardához fordult, és második véleménye volt, glaukóma és szaruhártyaödéma volt. Timolol/dorzolamid/brimonidin kezelés alatt állt.
Dr. Balparda DSAEK típusú lamelláris műtétet végzett a jobb szemében, jó kezdeti evolúcióval, de a korai posztoperatív időszakban folyadék kezdett felhalmozódni a felületen (kép).
Abbahagyta a szteroid kezelést, és latanoprostot és orális acetazolamidot adott hozzá a korábbi antiglaukóma kezeléshez anélkül, hogy javulást mutatott volna. Úgy döntött, hogy megemeli a fedelet, hogy visszahelyezze, ez a technika eredetileg sikeres volt, amíg a műtétet követő 72 óra elteltével a folyadék ismét elkezdett felhalmozódni az interfészben.
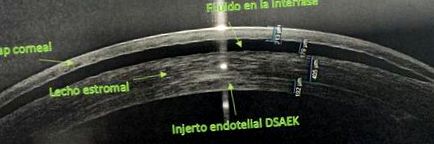
A javasolt terápiás lehetőségek:
- A kortikoszteroidok felfüggesztése: Amint Dr. Balparda már megtette
- A glaukóma orvosi kezelése: megpróbálják elkerülni a karboanhidráz inhibitorokat az endoteliális elváltozások elkerülése érdekében
- Szelektív lézeres trabeculoplasztika (STL)
- Szűrő műtét: Trabeculectomia vs Ahmed szelepe
BEVEZETÉS
A lézeres asszisztált keatomileusis (LASIK) manapság a legszélesebb körben elvégzett fénytörési technika. (1) Becslések szerint több mint 16 millió embernél hajtották végre ezt az eljárást 1990-es bevezetése óta. (2) A technika népszerűségének köszönhető mindkét myopia kezelésének kiváló hatékonysága, biztonsága, stabilitása és kiszámíthatósága, például mint hiperopia, asztigmatizmussal társítva vagy nem. (3.5)
Idővel az eredmények a technológiai fejlődés eredményeként javultak. (4,6) Mindenekelőtt a szaruhártya fedél létrehozása, amely egy mechanikus mircokeratométerrel (MK) egy femtoszekundumos lézerrel (LFS) történt. Úgy tűnik, hogy az LFS előnyöket nyújt az MK-val szemben, például egy vékonyabb, egységesebb és pontosabb fedél létrehozásának lehetőségét, csökkentve az intraoperatív és a posztoperatív szövődményeket. (1)
A LASIK műtét után előforduló komplikációk között szerepelnek a fedéllel, a hám növekedésével a felületen, a diffúz lamelláris keratitis, a fertőzések, a felületen lévő tályogok vagy a felületen lévő folyadék felhalmozódása, más néven folyadék szindróma. . (7,8,9)
Lyle és Jin 1999-es leírása óta (12) az IFS számos nevet kapott etiológiájával és patogenezisével kapcsolatos ismeretek hiánya miatt; A nyomás okozta intralamelláris stroma keratitis, a szteroidok által indukált lamelláris keratopathia és az intralamelláris stromális keratopathia neveket használták ennek az entitásnak a megnevezésére. Mindegyikük az IFS különböző stádiumú, de ugyanahhoz a folyamathoz tartozó jeleit és tüneteit képviseli, amint azt Dawson és munkatársai tanulmányukban bemutatták. (11) 2012-ben Galvis V és munkatársai a LASIK utáni ödéma által kiváltott keratopathia (PELK) nevét javasolták erre az entitásra (10), ahol a nyomás által kiváltott kifejezés nem szerepelt, mert nem csak IOP emelkedett de minden olyan patológia esetén, amely a LASIK utáni szaruhártyaödémát okozza. A "folyadék" kifejezés szintén nem szerepel benne, mivel a réslámpa vizsgálatakor nem mindig találunk nyilvánvaló folyadékot.
Az IFS-t a vizes humor felhalmozódása jellemzi az intrastromális térben, amely általában a műtétet követő első hét és néhány hónap-év között jelenik meg. (12) Ennek oka lehet a kortikoszteroidokra reagáló betegek IOP-növekedése, korábbi endotheliális diszfunkció, uveitis, endotheliális vagy szaruhártya-trauma. (13,14,15)
Klinikailag diffúz, nem szemcsés homályt figyelhetünk meg, amely a LASIK központi területére korlátozódik. Ez a köd könnyen összetéveszthető a diffúz lamelláris keratitisben észlelt szemcsés homályral, amely az SFI-vel ellentétben klinikailag gyakoribb és általában a posztoperatív hét előtt jelentkezik. (tizenegy)
A réslámpában a szaruhártya fedele és a maradék sztróma között folyadék által elfoglalt teret figyelhetjük meg, amelyet az OCT-SA megerősíthet. Dawson és munkatársai (11) a réslámpában megfigyelt jellemzőknek megfelelően végeztek egy szakaszolást:
3. ábra: Dawson és mtsai által javasolt osztályozás. SFI, amelyet megnövekedett nyomás vagy endothel károsodás okoz.
- 1. szakasz: az interfész enyhe vagy közepes váladékozása érezhető köd nélkül.
- 2. szakasz: a felület mérsékelt-súlyos váladékozása diffúz mérsékelt-súlyos köddel társul, nem szemcsés és néha egy kis folyadékzseb.
- 3. szakasz: Nagy, diffúz zsák összefolyó folyadék, amely összegyűlik a LASIK fedél és a maradék stromális ágy között.
A különböző szakaszok a klinikai jellemzők részét képezik, amelyeket a LASIK által működtetett szaruhártyákban figyelhetünk meg, a szaruhártyaödéma súlyosságától és időtartamától, valamint az azt kiváltó mechanizmustól függően. (tizenegy)
Az IOP növekedése által okozott esetekben általában hamisan csökken, mert mérjük az interfészen meglévő nyomást. (16) A valós nyomás közelítőbb mérése érdekében perifériás szinten kell megvizsgálnunk a nyomást, amint azt Dr. Oscar Albis és Dr. Jorge Pacheco javasolja. (17)
Közzétett tanulmányok szerint a refrakciós műtéten átesett és a meg nem operált betegek között is ellentmondás van a központi és a perifériás IOP közötti összefüggésben. (17) Egyes tanulmányok szerint a szaruhártya temporális részén végzett mérés hasonló a műtét előtti központi méréshez, így megbízható mérés lehet műtött betegeknél. (18) Más vizsgálatok a centrális-perifériás 1,0-2,8 Hgmm közötti különbségeket figyeltek meg LASIK-betegeknél. Ez a különbség összefüggésbe hozható a szaruhártya behatolással szembeni ellenállásának csökkenésével, akár a szaruhártya stromájának elvékonyodása, akár bowman membrán ablációja miatt. (19)
Az iridián implantátumokat 1956-ban tervezték a veleszületett vagy traumás írisz-hibák (aniridia, írisz-coloboma, szemi albinizmus stb.) Kijavítása céljából, annak érdekében, hogy csökkentsék a tükröződést és a fényérzékenységet. (24)
A NewIris kozmetikai implantátumokkal kapcsolatos szövődmények közül a szaruhártyaödéma, az okuláris hipertónia (OHT), a pigment diszperzió, az uveitis, az endothelsejtek számának csökkenése, az Uveitis-Glaucoma-Hyphema (UGH) szindróma, a glaucomatous opticus neuropathia, a trabecularis háló és az elülső synechia kialakulása . Ezeket a szövődményeket Dr. Dante Buonsanti és Dr. Luis W LU javasolta. (20,21,22,23) 2012-ben Rupa D. Shah és J. Bradley Randleman orvosok az Elsevier kiadóhoz írtak figyelmeztetést a NewColorIris Implants készülékek okozta súlyos szövődményekre. (25)
Dr. Garcia-Pous, a valenciai egyetemről, Panamában publikálta egy 21 éves lány esetét, akinek az írisz színének megváltoztatására kozmetikai műtéten esett át. (21) A műtét után a betegnél glaukóma és a szaruhártya endotheliumának dekompenzációja alakult ki, amely orvoskezeléssel és az írisz implantátum eltávolításával megoldható volt. A cikkben közzétett képeken láthatjuk, hogy néz ki a NewIris implantátum (ábra). Az OCT-SA-ban megfigyeltük, hogy ebben az esetben hogyan érintkezik közvetlenül a szaruhártya endotheliummal és hogyan akadályozza a trabecularis hálót. (huszonegy)
4. ábra: Dr. García-Pous cikkében közzétett kép. Megjelenik a NewIris eszköz alakja. 11-13 mm átmérőjű szilikon implantátum 3,5 mm és 0,16 mm vastag pupilla nyílással. Úgy tervezték, hogy beültesse az elülső kamrába. 5. ábra. Elülső kamra optikai koherencia tomográfia, amely az íriszen nyugvó és a trabecularis hálóval érintkező NewIris implantátumot mutatja.
Jelenleg ezeket az eszközöket csak Panamába ültetik be, anélkül, hogy azokat az FDA jóváhagyta volna az Egyesült Államokban, vagy hogy a CE-jelölés Európában lenne. (25) Ezért fontos, hogy figyeljünk a konzultáción esetleg megjelenő lehetséges betegekre.
A fórumon felvetett lehetséges terápiás lehetőségek között a következőket találjuk:
Először is, a kortikoszteroidokat el kell választani a kortikoszterápiára reagáló betegeknél, hogy elkerüljék az intraokuláris nyomás növekedését, ahogy Dr. Balparda tette. Ez nagyon fontos, mivel, mint tudjuk, a refrakciós műtéten átesett betegek többsége myopiás, és hajlamosabbak az OHT kialakulására a szteroidos kezelés után. (17)
Másodszor, antiglaukomatikus orvosi kezelést választanánk, ha a kortikoszteroidok visszavonása után nem érhető el az IOP csökkenése, és megpróbálnánk elkerülni a karboanhidráz inhibitorok (IAC) alkalmazását, amint arra Dr. Luis W LU rámutatott, és a legtöbb fórumként orvosok. Az IAC-k képesek csökkenteni a bikarbonát-ionok képződését a sejtben, csökkentik a kapcsolódó nátrium- és vízszállításokat, és ezáltal szaruhártya-ödémát okozhatnak a gyenge endotheliális funkcióval rendelkező szemekben, és késleltethetik a stromális folyadék kiürülését. (29.30)
Harmadszor, a szelektív lézeres trabeculoplasztikát javasolták közbenső lépésként a végleges műtétig.
A szűrési műtét lenne az utolsó lépés a kontrollálhatatlan glaukóma kezelésében.
Egy nemrégiben készült tanulmányban retrospektív elemzést végeztek 87 szemen, amelyeket kétféle írisz színváltó eszközzel (New Color Iris és Bright Ocular) telepítettek, mindkettő FDA jóváhagyás vagy CE jelölés nélkül. Az operált szemek 92,3% -ának volt legalább egy szövődménye (31), és ezek közül 54,1% -nál OHT alakult ki, többségük négyszeres terápiát és szisztémás kezelést igényelt. Ebben a vizsgálatban tizenöt szemnek (23,1%) szűrési műtétet kellett elvégeznie. (31) Ezt a lehetőséget ajánlották a fórum orvosai a legjobban, és a bemutatottakhoz hasonló esetekben a legtöbb gyakorlatot. (16,34,35)
Fontos, hogy keressük az IFS másodlagos okát, például egy korábbi endotheliális dekompenzációt, bár ezt kezdetben esetünkben a Dr. Balparda által végzett lamináris műtét (DSAEK) vagy az uveitis kizárta. Dr. El Chebab és munkatársai azt mutatják, hogy a betegek csaknem 40% -ában jelen lehet ilyen típusú eszköz. (31)
Dr. Balparda a Flap amputációjáról kérdezte:
Bár ez egy olyan technika, amelyet végső megoldásként tartanak fenn, és a konzervatív kezelésre nem képes betegek számára, hasznos lehet olyan bonyolult esetekben, amelyek nem reagálnak a kezelésre. (32) A szárny amputálásának célja, hogy az új hám be tudja fedni a szabadon fekvő stromális ágyat, és szabályos felületet teremtsen, hasonlóan a szaruhártyához, amely a fotorefraktív keratectomia (PRK) után marad. Ennek az új felületnek stabil fénytörést és helyes látásélességet kell biztosítania. A fedél eltávolításának lehetősége nem jelentene végleges megoldást a bemutatott esetre, mivel - Dr. Galvis V leírása szerint - az IFS másodlagos az OHT által termelt szaruhártyaödéma miatt.
Fontos szempontok
- Legyen figyelmes az irídiai kozmetikai implantátummal rendelkező betegekre a később esetlegesen kialakuló szövődmények miatt; szaruhártya dekompenzáció az endothel sejtek elvesztése, uveitis, glaucomatous opticus neuropathia stb. (2. 3)
- Az IFS etiopatogenezise bármely olyan szembetegségnek köszönhető, amely szaruhártyaödémát okoz. Mivel ez nem gyulladásos betegség, a kortikoszteroidokkal történő kezelés nem javallt, és ronthatja az állapotot. (10)
- Az IFS diagnózisának késése visszafordíthatatlan látásvesztéshez vezethet. (13)
Ezt a betegséget mindig figyelembe kell venni, amikor diffúz köd jelenik meg, keressen folyadékot a határfelületen, és vegye figyelembe az intraokuláris nyomást a periférián, ellentétben a diffúz lamináris keratitisszel, ahol a köd a kezelt optikai zónában marad, az SFI-ben ez az egész a szaruhártya. (10.16)
