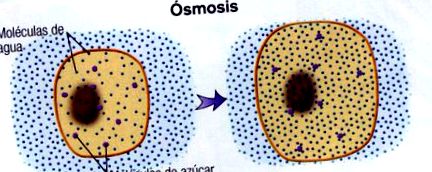
Az ozmózis nagyon fontos folyamat kémiai és biológiai szinten egyaránt.
De, Mi az ozmózis? Az ozmózis olyan jelenség, amikor az oldószer áthaladása vagy diffúziója egy félig áteresztő membránon keresztül történik, amely lehetővé teszi az oldószer áthaladását az oldott anyagtól nem, a hígabb oldatból a koncentráltabbá.
A víznek a féligáteresztő membránként viselkedő plazmamembránon való áthaladásának képessége az extracelluláris és intracelluláris folyadékok koncentrációjának különbségétől függ, és ásványi sók és oldott szerves molekulák jelenléte határozza meg.
A féligáteresztő membránok által elválasztott vizes közeg különböző koncentrációjú lehet, és ezeket nevezik:
- Hypertonikus, azok, amelyekben az oldott anyagok koncentrációja magas, összehasonlítva másokkal, amelyekben a koncentráció alacsonyabb.
- Hipotóniás, azok, amelyek alacsony koncentrációban tartalmaznak oldott anyagokat, összehasonlítva másokkal, amelyekben ez magasabb.
A vízmolekulák a hipotóniától a hipertóniás közeg felé diffundálnak, ami megnöveli a nyomást a hipotonikus rekesz membránjának felületén, az ún. ozmotikus nyomás. Az ozmotikus folyamat eredményeként egyensúly érhető el, a koncentrációk kiegyenlítődnek, majd a közeg izotóniás, vagyis azonos a koncentrációjuk.
Ozmózis a konyhában
Nincs tudomásunk, de a konyhánkban láthatjuk az ozmózist: amikor tésztát vagy rizst főzünk, amikor ráncos burgonyát készítünk, saláta leveleket vagy hüvelyeseket áztatunk
Ha száraz salátalevelet teszünk vízbe, akkor néhány órán belül helyreállítja az összes állagát. A saláta elvesztette vizét, és az ozmózisnak köszönhetően visszanyeri azt.
Ennek a ténynek a bizonyítására nagyon egyszerű kísérlet végezhető két csirketojással, ecettel és két oldattal: az egyik erősen koncentrált valamilyen oldott anyagban (például sóban), a másik pedig csak desztillált vízzel.
Amint azt a kísérlet során láthatjuk, a nagyon sós (hipertóniás) oldatban lévő tojás hajlamos arra, hogy a vizet eldobja, ráncosabbá váljon, míg desztillált vízben (hipotonikus oldat) felfújódik. Ugyanez a kísérlet elvégezhető különböző koncentrált oldatok sónál nagyobb oldott anyagokkal történő tesztelésével és a hatás drasztikusabb megfigyelésével (például glükózsziruppal vagy cukorral).
Az a hidrosztatikus nyomás, amelyet a víz be- vagy kilépésre gyakorol, ozmotikus nyomásnak nevezi, és a koncentrációk és a hőmérséklet szabályozza.
Mi történne a sejtjeinkkel?
A következő videókban vörösvérsejteket láthat hipertóniás és hipotonikus oldatokban. Amikor a vörösvérsejtek hipertóniás oldatban vannak, a koncentráció kiegyenlítése érdekében víz szabadul fel, "száraz" marad, ami halálukat okozza.
Ha az oldódás hipotóniás, a vörösvérsejtek hajlamosak vizet felvenni és megduzzadni, néha sejtrepedést vagy lízist okozva.
A következő képek a következő tapasztalatok eredményét mutatják:
Ugyanazon személy vörösvértestjeit három különböző megoldásban vezették be:
- Izotóniás. Az eritrocitákat egy vérszérumot tartalmazó tartályban helyezték el.
- Hipotóniás Az eritrocitákat egy vízzel hígított vérplazmát tartalmazó edénybe vezettük.
- Hypertonikus Az eritrocitákat egy vérplazmát tartalmazó tartályba helyezték, amelyhez koncentrált NaCl-oldatot adtak.