Tárgyak
Összegzés
Fő
A glioblastomák (GBM) az elsődleges agydaganatok leggyakoribb formái, amelyek bármilyen korú felnőtt betegeket érinthetnek. Ezek az erősen vaszkularizált és beszűrődő daganatok rezisztensek a jelenlegi terápiákkal szemben, és leggyakrabban kevesebb, mint 18 hónap alatt végzetes eredményhez vezetnek. A jelenlegi sugárterápiás kezelés és a temozolomid alkalmazása jobb eredményeket nyújt az MGMT gén metilált profiljával rendelkező betegek számára. 16, 17 E kezelés hatékonysága azonban még antiangiogén molekulák (bevacizumab) alkalmazásával is korlátozott, és ez a tumor továbbra is gyógyíthatatlan marad. A GBM agresszív viselkedését, beleértve a jelenlegi kezelésekkel szembeni rezisztenciát és a daganat kiújulásait, a GBM-szerű progenitor sejtek (GSC) jelenlétének tulajdonítják. 18,19 Ezért sürgősen ki kell dolgozni olyan új kezelési módszereket, amelyek kifejezetten a GBM-szerű őssejteket célozzák meg e gyógyíthatatlan daganatok felszámolására.
MikroRNS profilalkotó megközelítést alkalmazva a betegből származó, glioma-szerű sejtek (GSC) elsődleges tenyészeteinek gyűjteményében, kimutattuk, hogy a miR-302-367 klaszter visszafordíthatatlan differenciált állapotba hozza a CMS-t, és blokkolja daganatok iniciálásának és előrehaladásának képességét in vivo. 20 Jelen tanulmányban megmutatjuk, hogy a páciens eredetű GSC, amelyet arra terveztek, hogy stabilan és konstitutívan kifejezze a miR-302-367 klasztert, képes volt felszabadítani a miR-302-367 tartalmú exoszómákat. Ezeket az exoszómákat a szomszédos GSC gyorsan internalizálta, ami a proliferáció és a proliferációs tulajdonságok megváltozásához vezetett miR-302-367-függő módon. A miR-302-367-et és a GSC-t expresszáló sejtek ortotóp xenograftja hatékonyan megváltoztatta a daganat fejlődését az egerek agyában, bemutatva annak terápiás potenciálját a daganat kiújulásának blokkolásában. Vizsgálatunk szerint a sejtalapú terápia innovatív megoldás lehet a rák ellen.
Eredmények
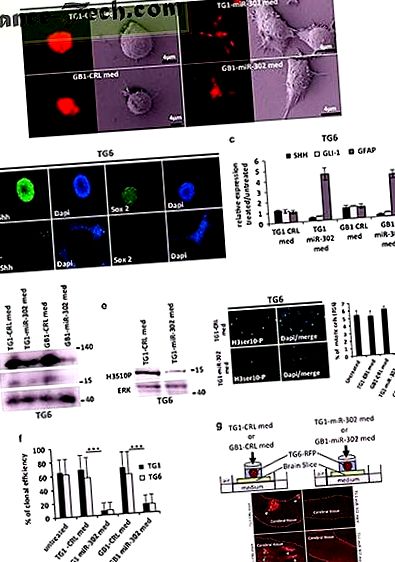
A miR-302 csoportot expresszáló GSC parakrin módon elnyomja az SHH és SOX2 expresszióját, proliferációját és beszivárgását
Teljes méretű kép
A TG1-miR-302 és GB1-miR-302 sejtek olyan exoszómákat választanak ki, amelyek képesek elnyomni a GSC potenciáját és proliferációját
A daganatellenes hatásért felelős molekulák azonosításához ultraszűrést hajtottunk végre a kondicionált táptalaj nagysága alapján. Megjegyezzük, hogy a nagy molekulatömegű frakció (
Teljes méretű kép
Teljes méretű asztal
A miR-302 klaszter exoszóma szekréció útján kerül a szomszédos sejtekbe
Teljes méretű kép
Teljes méretű asztal
A miR-302 csoport expressziója a GSC-ben elősegíti a parakrin tumor szupresszor hatását in vivo
Ennek a megközelítésnek az eredményei, amelyeket egereken kaptunk, bizonyítják azt az elvet, hogy a rák kezelésére szolgáló sejtalapú terápia megfontolandó. A GSC-n kívül más exoszómát szekretáló sejteket, például makrofágokat is izolálhatunk a betegektől, és genetikailag módosíthatjuk, hogy stabilan expresszálják a terápiás RNS-molekulákat tumorok kezelésére.
Ezeknek a sejteknek a műtét során közvetlenül a tumor helyére történő transzplantációja lehetővé tenné a tumor szuppresszor exoszómák hosszabb ideig tartó helyi beadását, elkerülve az exoszómák súlyos és stresszes időszakos injekcióit a betegbe.
Összegzésképpen úgy gondoljuk, hogy tanulmányunk felkelti az érdeklődést egy sejtalapú terápia iránt a terápiás exoszómák in situ szállítására az emberi GBM megcélzásához.
Anyagok és metódusok
Elektron mikroszkóp
Dinamikus fényszórás (DLS)
A DLS mérést egy Zetasizer Nano-ZS-szel (Malvern Instruments, Malvern, Egyesült Királyság) végeztük. A mintákat 100 μl 1 × PBS-ben hígítottuk. 3 × 12 méréssorozatot végeztünk standard beállításokkal (törésmutató = 1,33, hőmérséklet = 25 ° C, viszkozitás = 0,88882 és dielektromos állandó = 79,0). Az eredményeket az OriginPro 2015 segítségével ábrázoltuk.
Mikrovezikulás extrakció.
10 6/ml GSC meghatározott mikrovezikulák nélküli táptalajban (NS34 + táptalaj, Fareh és mtsai.). 72 óra elteltével a GSC-ket centrifugálással eltávolítottuk (276xg, 4 ° C, 5 percig), és a kondicionált táptalajt összegyűjtöttük, 0,2 μm-es szűrőn (Millipore, Fontenay sous Bois, Franciaország) átszűrtük és bepároltuk. 100 kDa-os Amicon Ultra centrifugális szűrővel (Millipore,). A koncentrált kondicionált táptalajt használtuk a mikrovezikulák tisztítására ultracentrifugálással 200 000 x g sebességgel 110 percig.
Reagensek és antitestek.
Sejtkultúra-reagenseket, köztük DMEM, F12, glutamin, Hepes, nátrium-hidrogén-karbonát, N2, G5 és B27, pENTR klónozó készletet, LR Clonase II, Superscript II reverz transzkriptáz, DiIC16 (3), DiO16 (3) és TRIzol reagenseket vásároltunk a Life Technologies-től (Cergy Pontolse, Franciaország). A magzati borjúszérumot (FCS) a Hyclone-tól (Brebières, Franciaország), az Exoquick készletet pedig az Ozyme-tól (St. Quentin, Yvelines, Franciaország) vásárolta meg. A Hoechst 33342-t és az Actinomycin D-t a Sigma (St. Quentin Fallavier, Franciaország) szállította, a Micromount Mounting Media-t pedig a Leica Biosystems-től (Nanterre, Franciaország) szerezte be. A Taqman reverz transzkripciós mikroRNS készletet, az Universal Taqman PCR Master Mix és a Taqman szondákat az Applied Biosystems-től (Villebon sur Yvette, Franciaország) szereztük be. A továbbfejlesztett kemilumineszcencia detektáló reagenst a Bio-Rad-tól (Marnes la Coquette, Franciaország) szerezték be.
Az ebben a vizsgálatban használt antitesteket itt soroljuk fel: poliklonális kecske anti-Shh (1/50 °, sc1194, Santa Cruz Biotechnology, Santa Cruz, Németország); Egér monoklonális anti-CXCR4 (1/50, MAB 172, R&D Systems, Egyesült Királyság); Nyúl poliklonális anti-H3-foszfo-S10 (1/100 °; ab5176, Abcam, Párizs, Franciaország); Anti-sox 2 poliklonális nyúl (1/100 °; Sox-2 (H65), sc-20088, Santa Cruz Biotechnology, Inc.); Egér monoklonális anti-Nestin (1/100 °, ab22035, Abcam); Kecskeellenes Alexa 488 (1/500 °; Düsseldorf, Németország); Alexa 488 nyúlellenes (1/500 °, Düsseldorf, Németország); Egérellenes Alexa 488 (1/500 °, Düsseldorf, Németország); Kecskeellenes Alexa 546 (1/500 °, Düsseldorf, Németország); Alexa 546 nyúlellenes (1/500 °, Düsseldorf, Németország); Egérellenes Alexa 546 (1/500 °; Düsseldorf, Németország); Anti-GFAP (1/200 °, 2203PGF, EUROPROXIMA, Arnhem, Hollandia). Anti-PTGFRN (1/500 °, ab174180, abcam); Anti-CD81 (1/500 °, klón # 454720, K + F rendszerek, Abingdon).
A miR-302a, miR-302b, miR-302c és miR-302d célzású miRCURY LNA Knockdown szonda kombinációt az EXIQON-tól (Madrid, Spanyolország) vásároltuk. Kódolt szekvenciát használtunk kontrollként.
Sejtkultúra
A GSC TG1, TG6 és GB1 primer sejtvonalakat izoláltuk a humán GBM-ből, ahogy azt máshol leírják. 20, 33, 34 Önmegújuló GSC-ként fenntartva a neuroszférákat NS34 + táptalajban tenyésztettük, amely EGF-et és bFGF-et tartalmazott (1/1 DMEM-F12 arány, 10 mM glutamin, 10 mM Hepes, 0 nátrium-hidrogén-karbonát, 025%, N2, G5 és B27). A sejtdifferenciálódáshoz szükséges táptalaj (MFCS) DMEM-F12-t, 10 mM glutamint, 10 mM Hepes-t, 0,025% nátrium-hidrogén-karbonátot és 0,5% FCS-t tartalmazott. Differenciálási kísérletek során a neuroszférákat disszociálták, és 500 000 egyedi sejtet tenyésztettek MFCS-ben.
Stabil plazmid és sejtvonal konstrukciók.
A miR-302 készletet genomiális humán DNS-ből amplifikáltuk PCR-rel (előreindító: 5'-GGCTGAAGTCCCTGCCTTTTACCC-3 ', reverz primer: 5'-TGGCTTAACAATCCATCACCATTGC-3') és kereskedelmi pENTR (élő technológia) vektorba klónoztuk. A 2K7 blasztidin (2K7BSD) lentivirális vektorba szubklónozást rekombinációval hajtottunk végre LR klonáz II jelenlétében. Az shLuc (2K7BSD-shLuc-scb) véletlenszerű formáját alkalmaztuk, amely megakadályozza a luciferáz gén, mint nem releváns konstrukció (CRL) gátlását. A lentivirális részecskéket úgy állítottuk elő, hogy a 293 T sejtvonalat 2K7BSD-Cluster mir-302 vagy 2K7BSD-shLuc-scb konstrukciókkal és a csomagoló vektorokkal (Invitrogen, Waltham, USA) transzfektáltuk. Lentivirális fertőzés után a miR-302 csoportot stabilan expresszáló sejtvonalakat (TG1 miR-302 csoport és GB1 miR-302 csoport) vagy az shLuc-scb kontrollt (TG1-CRL és GB1-CRL) blasztidint (1) tartalmazó közegben választottuk ki. μg/ml) 15 napig. Két stabil sejtvonalat fejlesztettek ki független vírusprodukciókból/fertőzésekből, és hasonló viselkedést mutattak. Az RFP-t stabilan expresszáló sejteket a GSC-k 2K7BSD-RFP lentivirális részecskékkel való fertőzését követően kaptuk.
Immunfluoreszcencia
A sejteket poli-L-lizinnel bevont üveg fedőlapokon növesztettük NBE, MFCS vagy kondicionált táptalajon. A megadott időpontokban a sejteket metanollal fixáltuk 10 percig -20 ° C-on, és előzőleg kétszer lehűtött PBS-sel mostuk. Az antitest blokkolást és hibridizációt 10% FCS-t és 0,1% Triton x 100-at tartalmazó PBS-ben hajtottuk végre. Az elsődleges antitestekkel szobahőmérsékleten végzett inkubálás után a sejteket háromszor PBS-sel mostuk, és szobahőmérsékleten 30 percig festettük fajokkal. . Specifikus szekunder antitestek fluoroforhoz kapcsolva. Ugyanakkor a magokat Hoechst 33342-vel (1 μg/ml) festettük. A tárgylemezeket kétszer PBS-sel, egyszer desztillált vízzel mostuk, végül Gel Mount oldattal szereltük fel. Az immunfluoreszcencia és az áteresztő fényképeket Nikon eclipse Ti mikroszkóppal készítettük (Nikon, Champigny sur Marne, Franciaország).
Klonogén vizsgálat
A neuroszférákat 20-szor disszociáltuk, óvatosan fel és le pipettázva az egyes sejteket. Általában 10 sejtet oltottunk minden lyukba 96-lyukú lemezeken, amelyek kontroll táptalajt vagy kondicionált miR-302-t tartalmaztak. 21 napos inkubálás után mindegyik üreget megvizsgáltuk, és megszámoltuk a neutroszférák számát. A kísérleteket három egymástól függetlenül megismételtük.
Kvantitatív valós idejű RT-PCR
Az RNS-t Trizol reagenssel extraháltuk. A mikroRNS és mRNS expressziós szinteket kétlépéses valós idejű RT-PCR-rel számszerűsítettük. A reverz transzkripciós lépéseket Superscript II reverz transzkriptázzal és Taqman reverz transzkripciós mikroRNS készlettel hajtottuk végre az mRNS és a miRNS számára, a gyártó utasításainak betartásával. Valós idejű PCR kísérleteket az univerzális Taqman PCR master mix alkalmazásával hajtottunk végre. A gén expresszió normalizálásához belső kontrollként kis nukleoláris RNS SNORD54 (vagy U54) és GAPDH expressziót alkalmaztunk. A hajtásváltozásokat a kontroll körülmények között becsültük meg ΔΔCT módszerrel.
Ortotópos Xenograftok
2,10 5 stabilan luciferázt (TG1-luc) expresszáló TG1 sejtet szuszpendáltunk 5 μl Hanks-kiegyensúlyozott sóoldatban (Invitrogen), és egyoldalúan beültettük a NOD.CB17-Prkdcscid/NCrHsd hím sztriatumába (Harlan, Franciaország). A luciferázt expresszáló sejteket együtt injektáltuk TG1 sejtekkel, amelyek stabilan expresszálták a miR-302 csoport kódolt szekvenciáját (TG1-scrb), vagy stabilan expresszálták a miR-302 csoportot. A luciferáz-aktivitás lehetővé tette az élő állatok tumorfejlődésének nyomon követését. A sejtek túlélését és a tumor növekedését élő állatokban 120 napig monitoroztuk és mennyiségileg meghatároztuk a luciferáz aktivitás detektálásával az IVIS Lumina II rendszerrel (Caliper Life Sciences, Hopkinton, MA, USA).
Organotípusos tenyészet MBS
Az agyakat újszülött egerekből boncoltuk, 4% cerebrospinalis folyadék agarba ágyazva (124 mM NaCl, 3 mM KCl, 26 mM NaHCO3, 2 mM CaCl2, 1 mM MgSO4, 25 mM KH 2 PO, 25 mM KH 2 PO 4, 10 mM és 400 mm vastag szeletekre vágjuk vibratómával. A szeleteket Millicell-CM tenyésztőlemezre (0,4 μm) helyeztük, behelyeztük és több mint 3 hétig levegő-folyadék határfelületen tartottuk.
Paraffin
Agylemezzel ellátott egereket 4% paraformaldehiddel rögzítettük 20 percig szobahőmérsékleten, majd PBS-sel mostuk. A mintákat ezt követően a következő inkubációs sorrendben dehidratáltuk: 70% etanol 15 percig, kétszer; etanol 90% 15 perc; 95% etanol 15 perc; 100% etanol 5 percig, háromszor; Címke 5 perc.
Ex vivo tumorigenesis vizsgálat
Az RFP-t stabilan expresszáló TG1-CRL és TG1-miR-302 sejtek tíz neuroszféráját beoltottuk az MBS felső felületére, és 3 hétig tenyésztettük levegő-folyadék határfelület körülményei között. A sejteket 48 óránként kondicionált táptalajjal kezeltük. A sejtek beszivárgását és növekedését vékony metszeteken belül, az RFP jel követésével, Nikon Eclipse Ti mikroszkóppal követtük el.
- A túlsúly az anyatejben olyan változásokat eredményez, amelyek befolyásolják a csecsemők növekedését
- Kórház San Rafael Ozono Csalások, fantázia vagy terápiás blogok
- Az ételek jelentősége a gyermekek növekedésében - A mai anyák
- A táplálkozás fontossága a gyermekek növekedésében és fejlődésében - TERHESSÉG
- A nyaki fájdalom kezelése Su Jok terápiával